ЛЕКЦИЯ 1. ВОДА — УНИКАЛЬНОЕ ВЕЩЕСТВО. ГИДРОЛОГИЯ.
Вода — уникальное вещество
Вода, у тебя нет вкуса, нет цвета, нет запаха, тебя невозможно описать;
люди тобою наслаждаются, при этом не ведая, что ты есть такое…
Нельзя сказать, что ты необходима для жизни: ты есть сама жизнь
Антуан де Сент-Экзюпери
В 1780 г Кавендиш и Лавуазье установили, что вода – простейшее и устойчивое в обычных условиях химическое соединение двух атомов водорода и одного атома кислорода. Чистая вода представляет собой бесцветную прозрачную жидкость без вкуса и без запаха.
Почти все физико-химические параметры воды не имеют аналогов в природе. Некоторые из этих аномалий имеют определяющее значение для формирования климата и рельефа нашей планеты, жизни человека, животных и растений. Если бы не эти "ненормальные" свойства, живые организмы не могли бы сохранять температуру своего тела, усваивать питательные вещества, то есть жизнь на планете Земля в современной ее форме была бы просто невозможна!
Половина всей крови человека — чистейшая дистиллированная вода. Мышцы человека на 75% состоят из воды. Вода является важнейшим пищевым продуктом. Дегидратация, или потеря организмом воды, нарушает деятельность сердечно-сосудистой системы, клеточный метаболизм и терморегуляцию. Потеря всего 3% воды организмом лишает человека возможности бегать. Потеря 5% воды лишает возможности тренироваться. А потеря организмом 10% воды представляет опасность для жизни.
Физические свойства воды и их значение
· Плотность воды при переходе ее из твердого состояния в жидкое не уменьшается, как почти у всех других веществ, а возрастает. При нагревании воды от 0 до 4 градусов по Цельсию плотность ее увеличивается. При 4 градусах вода имеет максимальную плотность.При дальнейшем нагревании ее плотность снова уменьшается. Замерзание воды сопровождается не сжатием (как у других жидкостей), а наоборот – расширением. Затвердевая, вода становится менее плотной – поэтому лед плавает, а не тонет.
Лед тем самым защищает нижележащие слои воды от дальнейшего охлаждения и замерзания. Таким образом, жизнь в воде продолжается.
· Высокая, по сравнению с соединениями водорода с похожим молекулярным весом, температура и удельная теплота плавления (0 °C и 333,55 кДж/кг), температура кипения (100 °C) и удельная теплота парообразования (2250 КДж/кг).
· Высокая теплоёмкость жидкой воды. В ночное время, а также при переходе от лета к зиме вода остывает медленно, а днем или при переходе от зимы к лету так же медленно нагревается, являясь, таким образом, самым главным регулятором температуры на земном шаре.
· Высокая вязкость.
· Высокое поверхностное натяжение.
· Вода практически несжимаема.
· Отрицательный электрический потенциал поверхности воды.
Особенности физических свойств воды обусловлены водородными связями. Молекула воды несимметрична: три ядра образуют равнобедренный треугольник с ядрами водорода в основании и ядром кислорода в вершине (радиус молекул воды значительно меньше внутримолекулярного расстояния, т.е. молекулы воды “упакованы” не слишком плотно).
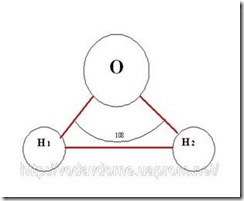
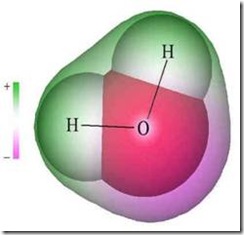
Из-за большой разности электроотрицательностей атомов водорода и кислорода электронные облака сильно смещены в сторону кислорода, тогда как 2 атома водорода в сумме формируют достаточно большую "площадь» распределения положительного заряда в "углах" молекулы. Несколько таких диполей будут образовывать структуры типа: Н2О...Н2О с водородной связью, когда между двумя атомами водорода будет втянут атом кислорода соседней молекулы. При этом общее распределение потенциала будет стремиться к минимизации взаимодействия с внешней средой, следовательно, молекулы воды будут располагаться в пространстве с чёткой ориентацией, в виде пространственных структур разной сложности: от спиралевидных (как у молекул ДНК) до пирамидальных, кубических, сферических разной сложности.
Каждая молекула воды может участвовать максимум в четырёх водородных связях: 2 атома водорода — каждый в одной, а атом кислорода — в двух. Простая, не объединившаяся с другой молекула воды H2O, называется гидроль, (H2O)2 — дигидроль, (H2O)3 — тригидроль. В парообразном состоянии вода в основном состоит из молекул гидроля, в жидком состоянии вода — смесь гидроля, дигидроля и тригидроля, во льду преобладают молекулы тригидроля. При таянии льда часть связей рвётся, при нагревании воды связи продолжают рваться, и плотность её растёт, но при температуре выше 4 °С этот эффект становится слабее, чем тепловое расширение. При испарении рвутся все оставшиеся связи. Разрыв связей требует много энергии, отсюда высокая температура и удельная теплота плавления и кипения и высокая теплоёмкость.
Вязкость воды обусловлена тем, что водородные связи мешают молекулам воды двигаться с разными скоростями. По сходным причинам вода является хорошим растворителем полярных веществ. Каждая молекула растворяемого вещества окружается молекулами воды, положительно заряженные участки молекулы растворяемого вещества притягивают атомы кислорода, а отрицательно заряженные — атомы водорода. Поскольку молекула воды мала по размерам, каждую молекулу растворяемого вещества могут окружить много молекул воды. Это свойство воды используется живыми существами. В живой клетке и в межклеточном пространстве вступают во взаимодействие растворы различных веществ в воде.[ Вода необходима для жизни всех без исключения одноклеточных и многоклеточных живых существ на Земле.
Чистая (не содержащая примесей) вода — хороший изолятор. Но поскольку вода — хороший растворитель, в ней практически всегда растворены те или иные соли, то есть в воде присутствуют положительные и отрицательные ионы. Благодаря этому вода проводит электричество. По электропроводности воды можно определить её чистоту. Она сильно поглощает инфракрасное излучение, и поэтому водяной пар является основным естественным парниковым газом, отвечающим более чем за 60 % парникового эффекта. Благодаря большому дипольному моменту молекул, вода также поглощает микроволновое излучение, на чём основан принцип действия микроволновой печи.
Гидрология и схема ее научных дисциплин
Предмет гидрологии
Гидрология– наука о воде (от греческого “hydro” — вода и “logos” учение, знание, наука). Гидрология — наука, занимающаяся изучением природных вод, явлений и процессов в них протекающих, закономерностей, по которым эти явления и процессы развиваются, закономерностей, определяющих распространение вод по земной поверхности и в толще почво-грунтов, а также их количественные изменения во времени.
Гидрология относится к комплексу наук, изучающих физические свойства Земли, в частности такой их элемент как гидросфера, то есть гидрология — часть физической географии — науки, занимающейся изучением явлений, происходящих на поверхности земного шара, формированием и динамикой их развития, взаимосвязями и закономерностями (physis — от греческого природа). Важным рубежом в истории развития гидрологии можно считать конец XVII в., когда французские ученые Пьер Перро, Эдм Мариотт и англичанин Эдмунд Галлей на основании измерений и расчетов осадков, стока и испарения впервые установили количественные соотношения главных фаз круговорота воды. В России более или менее систематические исследования водных объектов были начаты при Петре I.
Можно выделить объекты изучения гидрологии и в зависимости от объекта (в связи со специфическими особенностями процессов в них происходящих) — подразделы гидрологии:
- океаны и моря — гидрология моря — океанология;
— реки — гидрология рек — потамология; ![]() ГИДРОЛОГИЯ СУШИ
ГИДРОЛОГИЯ СУШИ
- озера и водохранилища — лимнология;
- ледники — гидрология ледников — гляциология — изучается в рамках физической географии;
- гидрогеология — входит в состав гидрологии поверхностных вод суши как вспомогательная дисциплина, в объеме, необходимом для установления взаимодействия поверхностных и подземных вод и влияния подземных вод на режим поверхностных вод.
- Prev
- Вперёд >>
